








Категория: Инструкции
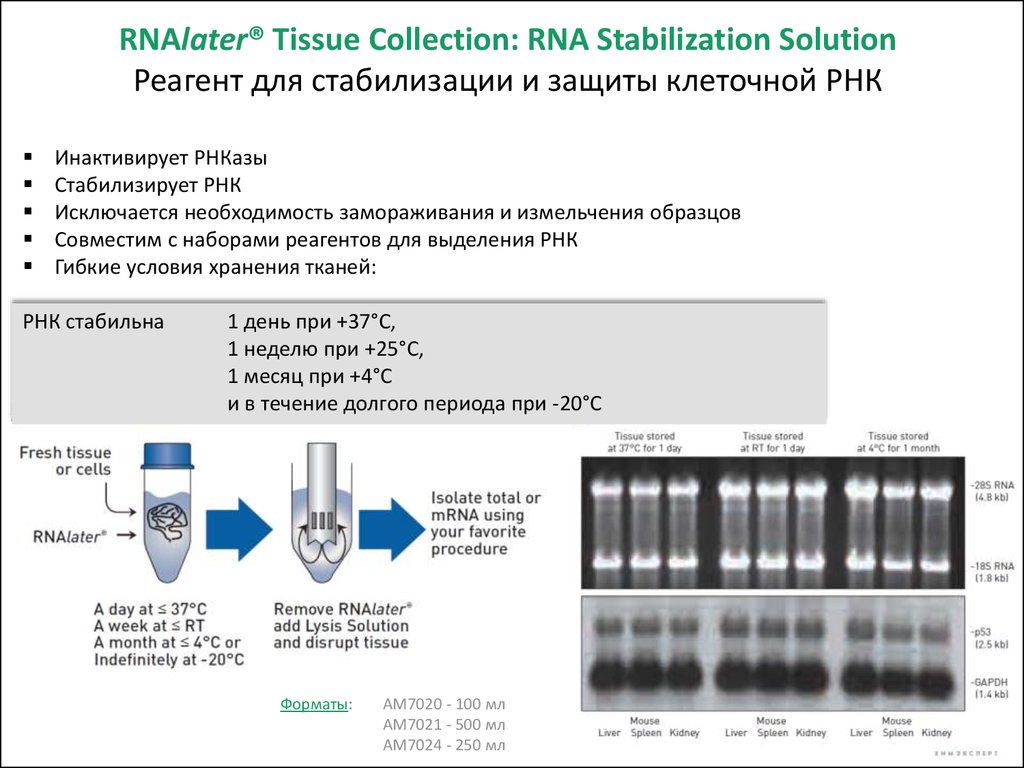
Ферментный препарат, получаемый из поджелудочной железы крупного рогатого скота. Деполимеризует РНК до кислоторастворимых моно- и олигопептидов. Разжижает гной, слизь, вязкую и густую мокроту; оказывает противовоспалительное действие. Разрушая нуклеиновые кислоты, задерживает размножение некоторых РНК-содержащих вирусов.
Активность рибонуклеазы определяют биологическим методом по количеству кислоторастворимых веществ, высвобождаемых в результате гидролиза РНК в определенных условиях. Одна единица активности (ЕА) соответствует 1 мг препарата.
Показания к применению— заболевания дыхательных путей с вязкой трудноотделяемой мокротой (бронхоэктатическая болезнь, абсцессы легких, ателектаз легкого, экссудативный плеврит);
— пародонтоз;
— гингивит;
— остеомиелит;
— свищи;
— абсцессы;
— трофические язвы;
— синусит (острый и обострение хронического);
— отит (острый и обострение хронического, в т.ч. в перфоративной стадии);
— тромбофлебит;
— клещевой энцефалит (при тяжелом течении заболевания, в сочетании со специфическим гамма-глобулином);
— вирусный менингит.
лиофилизат для приготовления раствора для инъекций и местного применения 10 мг; флакон (флакончик) 5 мл, пачка картонная 10;
Противопоказания к применению— хроническая сердечная недостаточность II-III стадий;
— туберкулез (открытая форма);
C осторожностью: эмпиема плевры (туберкулезной этиологии).
Побочные действияРаздражение слизистых оболочек дыхательных путей, аллергические реакции.
Способ применения и дозыПри местном применении присыпают раневую или язвенную поверхность порошком в количестве 25-50 мг и прикладывают салфетки или тампоны, смоченные раствором препарата в 0.9% растворе натрия хлорида.
Для ингаляций используют мелкодисперсный аэрозоль - 25 мг на 1 процедуру (для этого препарат растворяют в 3-4 мл 0.9% раствора натрия хлорида или в 0.5% растворе прокаина).
Эндобронхиально вводят раствор, содержащий 25-50 мг, при помощи гортанного шприца или катетера.
Внутриплеврально - 25-50 мг в 5-10 мл 0.9% раствора натрия хлорида или 0.2% раствора прокаина.
При синуситах - 5-10 мг в 3-5 мл 0.9% раствора натрия хлорида в верхнечелюстную (гайморову) пазуху после пункции и промывания; при отитах - 0.1% раствор (0.5-1 мл) в наружный слуховой проход.
В/м вводят 5-10 мг в 1 мл 0.9% раствора натрия хлорида или 0.5% раствора прокаина; курс лечения - 2-10 инъекций, по 1-2 инъекции в день.
Максимальная разовая доза при в/м инъекции - 10 мг, при местном и внутриполостном введении - 50 мг.
Для лечения клещевого энцефалита - в/м, 6 раз/сут, в разовой дозе - 25-30 мг; детям 1-3 лет - 5-8 мг (в зависимости от массы тела), 4-6 лет - 10-14 мг, 7-11 лет - 15-18 мг, 12-15 лет - 20 мг.
Необходимое количество препарата растворяют перед инъекцией в 2 мл 0.25-0.5% раствора прокаина. Перед началом лечения проводят пробы на чувствительность к препарату: на сгибательную поверхность предплечья вводят в/к 0.1 мл; терапию проводят при отсутствии местной и общей реакции.
Передозировка Особые указания при приемеРассасывание экссудата при эмпиеме плевры туберкулезной этиологии может способствовать развитию бронхоплевральной фистулы.
Условия храненияСписок Б. В сухом, защищенном от света месте, при температуре не выше 15 °C.
Срок годности Принадлежность к ATX-классификацииD Дерматотропные препараты
D03 Препараты для лечения ран и язв
D03B Ферментные препараты
D03BA Протеолитические ферменты




Автор-составитель: Эльвира Гиляева - врач, медицинский журналист Специализация: кардиология, функциональная диагностика, оториноларингология подробнее
Образование: Окончила Башкирский государственный медицинский университет по специальности "Лечебное дело". В 2011 году получила диплом и сертификат по Терапии. В 2012 году получила 2 сертификата и диплома по "Функциональной диагностике" и "Кардиологии". В 2013 году прошла курсы по "Актуальным вопросам оториноларингологии в терапии". В 2014 году прошла курсы повышения квалификации по специальности "Клиническая эхокардиография" и курсы по специальности "Медицинская реабилитация".
Опыт работы: С 2011 по 2014 год работала терапевтом и кардиологом в МБУЗ Поликлиника №33 г. Уфа. С 2014 года работает кардиологом и врачом функциональной диагностики в МБУЗ Поликлиника №33 г. Уфа.
ОБРАТИТЕ ВНИМАНИЕ! Информация о лекарствах на сайте является справочно-обобщающей, собранной из общедоступных источников и не может служить основанием для принятия решения об использовании медикаментов в курсе лечения. Перед применением лекарственного препарата Рибонуклеаза обязательно проконсультируйтесь с лечащим врачом.
Изобретение относится к области медицины и ветеринарии. Способ предусматривает использование рибонуклеазы бактериальной 7P для увеличения эффективности подавления размножения РНК- и ДНК-содержащих вирусов для лечения острых вирусных заболеваний млекопитающих и теплокровных животных. Преимущества заявляемой РНКазы заключаются в том, что подавление размножения вирусов РНКазой Bacillus intermedius достигается при использовании существенно более низких доз вводимых в инфицированный организм ферментов с повышенной эффективностью подавления размножения вирусов и лечебного процесса. 1 з.п. ф-лы, 8 табл. 7 пр.
Предлагаемое изобретение относится к области медицины и ветеринарии. Может быть использовано для подавления размножения вирусов, лечения млекопитающих и теплокровных - человека и животных - от заболеваний, вызываемых РНК и ДНК-содержащими вирусами.
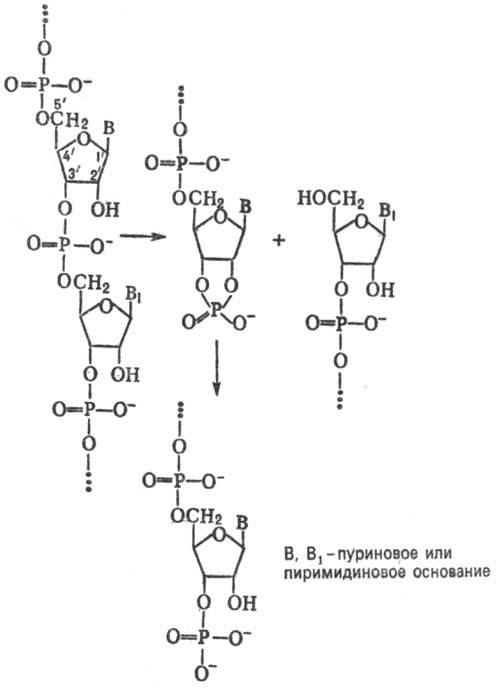
Рибонуклеазы (РНКазы) - ферменты метаболизма РНК, функции которых заключаются в расщеплении мРНК, превращении предшественников РНК в зрелые формы, образовании малых регуляторных РНК, деградации определенных типов РНК, в том числе вирусной РНК.
Известно [1] использование препарата с коммерческим названием «Эндоглюкин», состоящего из фермента - эндонуклеазы (бактериальной), продуцируемой бактериями Serratia marcescens - в смеси с полисахаридом полиглюкином. Недостатком [1] является существенная ограниченность области применения препарата - только для профилактики и лечения вирусных заболеваний пчел и стимуляции развития пчелиных семей. Для достижения других целей аналог неприменим. Кроме того, эндонуклеаза бактерий Serratia marcescens неустойчива в кислой среде и теряет активность, что также ограничивает область применения.
Известно [2] использование эндонуклеазы бактерии Serratia marcescens в качестве противовирусного препарата для оздоровления картофеля от вирусной инфекции при микроклональном размножении и создании трансгенных форм картофеля. Недостатком [2] является существенная ограниченность области применения препарата - только для профилактики и лечения вирусных заболеваний картофеля.
Общим недостатком аналогов [1] и [2] является то, что средство «Эндоглюкин» и эндонуклеаза Serratia marcescens не пригодны в качестве средства, подавляющего размножение вирусов человека и животных.
Известны результаты исследования рибонуклеазы Actynomices rimosus как возможного средства подавления развития вирусов человека и животных in vitro (в пробирке) [3]. Недостатком аналога [3] является то, что рибонуклеаза Actynomices rimosus не пригодна в качестве средства, способного подавлять размножение вирусов в организме животных.
Наиболее близким по существу заявляемого изобретения, прототипом, является способ подавления размножения вирусов человека и животных путем использования получаемого из поджелудочной железы крупного рогатого скота фермента - панкреатической РНКазы (далее по тексту - РНКаза ПЖ) [4].
Недостатком прототипа [4] является необходимость применения (для получения удовлетворительного результата) очень высокой разовой дозы вводимого в организм фермента. Так, при оценке противовирусной эффективности на новорожденных кроликах противовирусный эффект достигают при дозе фермента 135 200 мг/кг (10 мг/кролик; кролик весом 50 70 г). На мышах эффективная доза равна 250 мг/кг (5 мг/мышь; мышь весом 20 г). Для человека весом 60 70 кг для однократного результативного введения потребуется 10 15 г фермента на одну дозу, Общим недостатком применения прототипа [4] к различным теплокровным живым существам является обязательная для получения положительного результата (подавления размножения вирусов человека и животных) потребность использования удельно-высоких доз фермента (дозы на единицу массы подопытного объекта). Высокие дозы вводимого в организм фермента - чужеродного белка - приводят к нежелательным иммунологическим осложнениям (в организме). К осложнениям, существенным для сохранения здоровья и даже жизнеспособности организма, подвергающегося воздействию чужеродного белка.
Целью предполагаемого изобретения является повышение эффективности подавления размножения вирусов в инфицированном организме, снижение удельного количества и концентрации фермента, требуемых для подавления размножения вирусов, повышение результативности процесса подавления размножения вирусов, повышение лечебного эффекта.
Цели достигают тем, что для увеличения эффективности подавления размножения вирусов в инфицированном организме для лечения вирусных заболеваний используют бактериальный фермент - РНКазу Bacillus intermedius, биназу (далее по тексту - РНКаза Bi). Bacillus intermedius как вид на основе анализа 16S РНК по современной классификации относят к Bacillus pumilus (Gen Bank Accession № HQ 650161.1). Используют структурно идентичную РНКазе исходного штамма Bacillus intermedius 7P рибонуклеазу иных штаммов Bacillus intermedius и штаммов иных микроорганизмов. Термин «иные штаммы» означает селекционированные (клонированные) и инженерные штаммы.
Фермент, являющийся объектом изобретения, представляет собой, например, продукт жизнедеятельности известной бактерии Bacillus intermedius, гуанилспецифичную РНКазу с молекулярной массой 12,3 кДа, 109 аминокислотных остатков, pl=9,5. РНКаза Bacillus intermedius получена из культуральной жидкости Bacillus intermedius, например - штамма 7P, продуцента внеклеточной щелочной РНКазы [4].
Противовирусную активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) оценивают общеизвестными способами [6], например in vitro, и путем внутрибрюшинной и/или внутримышечной инъекции оцениваемых препаратов в организм животного. Примером наиболее часто применяемых для указанной цели (оценки действия исследуемого препарата) животных и/или их тканей являются морские свинки, свиньи, цыплята кур, мыши.
Заявляемое изобретение иллюстрируют примеры его применения в отношении наиболее типичных вирусов, например для воздействия на вирусы ящура (далее по тексту ВЯ), вируса болезни Ауэски (далее по тексту ВБА) и различных штаммов вируса гриппа. Приведенные примеры не ограничивают объем и сущность притязаний, связанных с ними.
Пример 1. Противовирусная активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) при заражении культуры клеток перевиваемых почек эмбрионов свиней (далее по тексту ППЭС) in vitro (в пробирке) РНК-содержащим вирусом ящура (далее по тексту ВЯ)
Оценку противовирусной активности РНКазы Bi и РНКазы ПЖ in vitro проводят следующим образом. Монослой 48-часовой культуры клеток ППЭС в пенициллиновых флаконах предварительно промывают раствором Хенкса, после чего заражают 0,1 мл суспензии ВЯ. Сразу же после заражения в одну часть флаконов с промытым монослоем клеток ППЭС добавляют разведенную средой роста РНКазу ПЖ (прототип), в другую часть флаконов - заявляемую РНКазу Bi. Флаконы оставляют в термостате при плюс 37°C на 1,0-1,5 часа и адсорбируют вирус испытуемыми клетками. После инкубации монослой клеток во флаконах с адсорбированным вирусом промывают раствором Хенкса. Раствор Хенкса после промывки инфицированного монослоя клеток сливают в сосуд сбора заразного материала для последующего уничтожения. Затем в эти же флаконы с монослоем, отмытым от не адсорбированного вируса, добавляют, например, в количестве 2 мл среду роста с соответствующими ферментами - РНКазой ПЖ или РНКазой Bi. Флаконы с монослоем вновь помещают в термостат при +37°. О размножении вируса судят по появлению цитопатогенного эффекта, который оценивают крестами от 1 до 4-х [5, 6]. Исследуемые клетки разрушают, например, путем замораживания и последующего оттаивания. Материал из опытных и контрольных флаконов после замораживания и оттаивания титруют [5, 6]. На каждые разведения берут по 4 пенициллиновых флакона. Результаты учитывают через 48 часов при заражении ВЯ и выражают в ТЦД 50 (тканевая цитопатическая доза, вызывающая разрушение 50% монослоя инфицированных клеток, рассчитываемых по Риду и Менчу)[5, 6]. В таблицах числовые значения ТЦД50 выражают в значениях десятичного логарифма (рассчитанных по Риду и Менчу числовых значений ТЦД50 ), Таблица 1.
Противовирусная активность РНКазы Bi (заявляемой) и РНКазы ПЖ (прототип) в культуре клеток ППЭС, инфицированных вирусом ящура (ВЯ). ТЦД50 - тканевая цитопатическая доза, вызывающая разрушение 50% монослоя инфицированных клеток
РНКаза Bi конечный титр вируса ящура снижает до значения Ig ТЦД 50 =2,1, РНКаза ПЖ - до значения Ig ТЦД50 =6,7 (снижение титра вируса РНКазой Bi от значений контроля составляет 5,4 Ig, РНКазой ПЖ - 0,8 Ig). Эффективность подавления размножения ВЯ РНКазой Bi без учета различий в дозах по активности и содержанию белка в три раза больше по сравнению с РНКазой ПЖ (6,7:2,1=3). Используемая доза заявляемой РНКазы Bi (60000 ед/мл или 0,08 мг/мл) в три раза меньше дозы прототипа РНКазы ПЖ (175000 ед/мл или 0,58 мг/мл) по активности (175000 ед. 60000 ед = 3) и в семь раз - по содержанию белка (0,58 мг. 0,08 мг = 7). Эффективность подавления размножения ВЯ РНКазой Bi по сравнению с РНКазой ПЖ с учетом различий в используемых дозах по активности выше в 9 раз (175000 ед. 60000 ед)×3=9, по белку - выше в 21 раз (0,58 мг. 0,08 мг)×3=21.
Пример 2. Противовирусная активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) при заражении культуры клеток перевиваемых почек эмбрионов свиней (далее по тексту ППЭС) in vitro (в пробирке) ДНК-содержащим вирусом болезни Ауэски (далее по тексту ВБА)
Оценку противовирусной активности РНКазы Bi и РНКазы ПЖ in vitro проводят следующим образом. Монослой 48-часовой культуры клеток ППЭС в пенициллиновых флаконах предварительно промывают раствором Хенкса, после чего заражают 0,1 мл суспензии ВБА. Далее выполняют действия, описанные в Примере 1. Результаты учитывают через 72 и 96 часов при заражении ВБА и выражают в ТЦД50. рассчитываемых по Риду и Менчу [5, 6]. В таблицах числовые значения ТЦД50 выражают в значениях десятичного логарифма (этих числовых значений ТЦД 50. рассчитанных по Риду и Менчу), Таблица 2.
Противовирусная активность РНКазы Bi (заявляемой) и РНКазы ПЖ (прототип) в культуре клеток ППЭС, инфицированных вирусом болезни Ауэски (ВБА).
ТЦД50 - тканевая цитопатическая доза, вызывающая разрушение 50% монослоя инфицированных клеток.
Доза фермента ед/мл(мг/мл)
РНКаза Bi снижает конечный титр ВБА до значения Ig ТЦД50 = 2,0, РНКаза ПЖ - до значения Ig ТЦД50 = 3,46 (снижение титра вируса РНКазой Bi от значений контроля составляет 3,25 Ig, РНКазой ПЖ - 0,8 Ig). Эффективность подавления размножения ВБА РНКазой Bi без учета различий в дозах по активности и содержанию белка в четыре раза больше по сравнению с РНКазой ПЖ (3,25:0,80=4). Используемая доза заявляемой РНКазы Bi (60000 ед/мл или 0,08 мг/мл) в три раза меньше дозы прототипа РНКазы ПЖ (175000 ед/мл или 0,58 мг/мл) по активности (175000 ед. 60000 ед = 3) и в семь раз - по содержанию белка (0,58 мг. 0,08 мг = 7). Эффективность подавления размножения ВБА РНКазой Bi по сравнению с РНКазой ПЖ с учетом различий в используемых дозах по активности выше в 12 раз (175000 ед. 60000 ед)×4=12, по белку - выше в 28 раз (0,58 мг. 0,08 мг)×4=28.
Пример 3. Противовирусная активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) при заражении мышей вирусом ящура
Работу с мышами выполняют по известной методике [5]. Оценку противовирусной активности на мышах проводят следующим образом. Берут десять групп белых беспородных мышей массой 18-20 г (в каждой группе по 10 животных), которым внутривенно вводят 100 ЛД50 (ЛД50 - летальная доза, вызывающая гибель 50% животных) ВЯ типа А22-50 ,адаптированного к этим животным. После заражения животным двух контрольных групп вводят изотонический раствор хлорида натрия, одной группе внутримышечно, другой - внутрибрюшинно.
Четырем группам инфицированных животных вводят заявляемую РНКазу Bi. Двум из них вводят фермент в дозе 15000 ед или 0,02 мг / 1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно. Двум оставшимся группам (мышей) вводят РНКазу Bi в дозе 17500 ед или 0,023 мг/1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно.
Четырем группам инфицированных животных вводят РНКазу ПЖ (прототип). Двум из них (групп) вводят фермент в дозе 60000 ед или 0,2 мг / 1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно. Двум оставшимся группам вводят РНКазу ПЖ в дозе 112000 ед или 0,35 мг/1,0 г массы мышей, одной группе внутрибрюшинно, второй группе - внутримышечно
Сравниваемые РНКазы вводят после заражения дважды в сутки, в течение 5 суток. О противовирусном действии ферментов судят по выживаемости животных. Результаты выражают в процентах по отношению к общему числу животных в группе (Таблица 3).
Противовирусная активность РНКазы Bi в дозе 15000 ед или 0,02 мг/на 1,0 г массы мышей колеблется в зависимости от способа вводимого фермента от 25 до 50% выживших животных. Продолжительность жизни животных, которым вводили фермент, но которые не вошли в группу выживших, колеблется от 3-х до 6-ти суток в зависимости способа введения фермента.
Противовирусная активность РНКазы ПЖ в дозе 60000 ед или 0,2 мг / на 1,0 г массы мышей, по активности в 4,0 раза превышающая дозу РНКазы Bi (60000 ед. 15000 ед = 4), а по белку превышающая в 10 раз (0,2 мг. 0,02 мг = 10) при внутрибрюшинном и внутримышечном способе введения не приводит к выживанию животных.
При внутрибрюшинном введении РНКаза Bi в дозе 17500 ед или 0,023 мг / на 1 г массы мышей обеспечивает выживание 30% животных. РНКаза ПЖ при внутрибрюшинном введении 112000 ед или 0,35 мг / на 1 г массы не приводит к выживанию животных.
При внутримышечном введении РНКаза Bi в дозе 17500 ед или 0,023 мг / на 1 г массы обеспечивает выживание 50% инфицированных животных, РНКаза ПЖ (прототип) при внутримышечном введении 112000 ед или 0,35 мг / на 1 г массы обеспечивает выживание 20% животных. Эффективность противовирусного действия РНКазы Bi в отношении ВЯ без учета различий в дозах по активности и содержанию белка в два с половиной раза больше по сравнению с РНКазой ПЖ (50%. 20% = 2,5). Используемая доза заявляемой РНКазы Bi (17500 ед/мл или 0,023 мг/мл) в шесть раз меньше дозы прототипа РНКазы ПЖ (112000 ед/мл или 0,35 мг/мл) по активности (112000 ед. 17500 ед = 6) и в 15 раз меньше по содержанию белка (0,35 мг. 0,023 мг = 15). Эффективность противовирусного действия РНКазы Bi по сравнению с РНКазой ПЖ (прототип), с учетом различий в используемых дозах, по активности больше в 15 раз (112000 ед. 17500 ед)×2,5=15, по белку - больше в 37,5 раз (0,35 мг. 0,023 мг)×2,5=37,5.
Пример 4. Оценка противовирусной активности в отношении вируса ящура на кроликах с использованием РНКазы Bi иного (по отношению к штамму Bacillus intermedius 7P) штамма
Работу с кроликами выполняют по известной методике [5]. Оценку проводят следующим образом. Берут десять групп по 10 новорожденных 4-5 дневных кроликов - две группы контрольные, восемь других - опытные.
Животных одной контрольной группы и четырех опытных групп заражают подкожно лапинизированным (адаптированным к кроликам) ВЯ штамм «0» с титром инфицирующего вируса 5,5 1д ТЦД 50 в 0,1 мл (исходный титр вируса на мышах-сосунках составляет 7,5 Ig ТЦД50 в 0,1 мл). Животным четырех опытных групп сразу после заражения вводят РНКазы. Двум группам животных РНКазу Bi в дозе 25000 ед или 0,033 мг / на 1,0 г массы кролика (одной группе внутрибрюшинно, другой - внутримышечно). Животным контрольной группы вместо фермента вводят изотонический раствор хлорида натрия.
В двух других группах животным вводят РНКазу ПЖ в дозе 100000 ед или 0,33 мг / на 1,0 г массы (в одной группе внутрибрюшинно, в другой - внутримышечно),
Животных второй контрольной группы и четырех опытных групп заражают подкожно лапинизированным (адаптированным к кроликам) ВЯ штаммом «0» с титром инфицирующего вируса 3,5 Ig в 0,1 мл. Животным четырех опытных групп сразу после заражения вирусом вводят РНКазы. Двум группам РНКазу Bi по 25000 ед или 0,033 мг/на 1,0 г массы (одной группе внутрибрюшинно, другой - внутримышечно). Двум другим группам вводят прототип - РНКазу ПЖ по 100000 ед или 0,33 мг / на 1,0 г массы (в одной группе внутрибрюшинно, в другой - внутримышечно).
РНКазы вводят 1 раз в сутки в течение 5-суточного периода наблюдения. Животным контрольной группы вместо фермента вводят изотонический раствор хлорида натрия. О противовирусном действии ферментов судят по выживаемости животных. Результаты выражают в процентах по отношению к общему числу животных в группе (Таблица 4).
Противовирусная активность РНКазы Bi (заявляемой) и РНКазы ПЖ (прототип) при заражении новорожденных кроликов вирусом ящура.
В скобках () - время гибели контрольных животных, которым вводят изотонический раствор хлорида натрия вместо фермента. В контроле, инфицированные вирусом с титром 5,5 Ig в 0,1 мл животные погибли все (100%). Среди инфицированных вирусом с титром 3,5 Ig контрольных животных погибло 80%
Условия оценки противовирусной активности
Титр инфицирующего вируса в Ig в 0,1 мл
Метод введения фермента
Время гибели животных, час
При инфицировании животных вирусом с титром 5,5 Ig в 0,1 мл противовирусная активность РНКазы Bi в дозе 25000 ед (или 0,033 мг/на 1,0 г массы) колеблется в зависимости от способа введения фермента в интервале 30-40% выживших животных. При этом инфицирующем титре вируса РНКаза ПЖ в дозе 100000 ед (или 0,33 мг/на 1 г массы), в 4 раза превышающей дозу РНКазы Bi по активности (100000 ед. 25000 ед = 4) и в 10 раз - по белку (0,33 мг. 0,033 мг = 10), при титре инфицирующего вируса 5,5 Ig в 0,1 мл, не приводит к выживанию животных.
При инфицировании животных вирусом с титром 3,5 Ig в 0,1 мл РНКаза Bi в дозе 25000 ед (или 0,033 мг / на 1,0 г массы) при внутрибрюшинном способе введения обеспечивает выживание 50% животных. При инфицирующем титре вируса 3,5 Ig в 0,1 мл РНКаза ПЖ при внутрибрюшинном введении в дозе 100000 ед (или 0,33 мг / на 1 г массы) в 4 раза превышающей дозу РНКазы Bi по активности (100000 ед. 25000 ед = 4) и в 10 раз по белку (0,33 мг. 0,033 мг = 10) при титре инфицирующего вируса 3,5 Ig в 0,1 мл обеспечивает выживание 20% животных. Противовирусная эффективность РНКазы Bi при внутрибрюшинном способе введения фермента без учета различий в используемых дозах ферментов выше противовирусной эффективности РНКазы ПЖ в 2,5 раза (50%. 20% = 2,5). С учетом различий в используемых дозах противовирусная эффективность РНКазы Bi при внутрибрюшинном способе введения выше противовирусной эффективности РНКазы ПЖ по активности в 10 раз (100000 ед. 25000 ед)×2,5=10, по количеству ферментного белка в 25 раз (0,33 мг. 0,033 мг)×2,5=25 При внутримышечном введении РНКаза Bi в дозе 25000 ед или 0,033 мг / на 1,0 г массы обеспечивает выживание 60% животных, РНКаза ПЖ, используемая в дозе 100000 ед или 0,33 мг / на 1 г массы, обеспечивает выживаемость 30% животных. Без учета различий в используемых дозах противовирусная эффективность РНКазы Bi выше противовирусной эффективности РНКазы ПЖ в 2,0 раза (60%. 30% = 2). С учетом различий в используемых дозах противовирусная эффективность РНКазы Bi выше противовирусной эффективности РНКазы ПЖ по активности в 8 раз (100000 ед. 25000 ед)×2=8, выше по белку в 20 раз (0,33 мг. 0,033 мг)×2=20.
Пример 5. Противовирусная активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) при заражении мышей вирусом болезни Ауески (ВБА).
Работу с мышами выполняют по известной методике [5]. Оценку противовирусной активности на мышах проводят следующим образом. Берут десять групп белых беспородных мышей массой 18-20 г (в каждой группе по 10 животных), которым подкожно вводят 10 ЛД50 (ЛД50 - летальная доза, вызывающая гибель 50% животных) ВБА, патогенного для лабораторных животных. После заражения животным двух контрольных групп вводят изотонический раствор хлорида натрия, одной группе внутримышечно, другой - внутрибрюшинно.
Четырем группам инфицированных животных вводят заявляемую РНКазу Bi. Двум из них вводят фермент в дозе 17000 ед или 0,02 мг / 1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно. Двум оставшимся группам мышей вводят РНКазу Bi в дозе 30000 ед или 0,035 мг / 1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно.
Четырем группам инфицированных животных вводят РНКазу ПЖ (прототип). Двум группам вводят фермент в дозе 65000 ед или 0,2 мг/1,0 г массы мышей, одной группе внутрибрюшинно, второй - внутримышечно. Двум оставшимся группам вводят РНКазу ПЖ в дозе 107250 ед или 0,33 мг / 1,0 г массы мышей, одной группе внутрибрюшинно, второй группе - внутримышечно
Сравниваемые РНКазы вводят спустя 1,0 час после заражения животных в течении 10 суток. После десятого введения РНКазы животных наблюдают еще 20 суток. О противовирусном действии ферментов судят по выживаемости животных. Результаты выражают в процентах по отношению к общему числу животных в группе (Таблица 5).
Противовирусная активность РНКазы Bi в дозе 17000 ед или 0,02 мг / на 1,0 г массы мышей колеблется в зависимости от способа вводимого фермента от 10 до 30% выживших животных. Продолжительность жизни инфицированных животных, которым вводили фермент, но которые не вошли в группу выживших, колеблется от 5-ти до 8-ми суток в зависимости способа введения фермента.
Противовирусная активность РНКазы ПЖ в дозе 65000 ед или 0,2 мг / на 1,0 г массы мышей, по активности в 3,8 раза превышающая дозу РНКазы Bi (65000 ед. 17000 ед = 3,8), а по белку превышающая в 10 раз (0,2 мг. 0,02 мг = 10), при внутрибрюшинном и внутримышечном способе введения не приводит к выживанию животных.
При внутрибрюшинном введении РНКаза Bi в дозе 30000 ед или 0,035 мг / на 1 г массы мышей обеспечивает выживание 30% животных. РНКаза ПЖ при внутрибрюшинном введении 107250 ед или 0,33 мг / на 1 г массы не приводит к выживанию животных.
При внутримышечном введении РНКаза Bi в дозе 30000 ед или 0,035 мг / на 1 г массы, обеспечивает выживание 50% инфицированных животных, РНКаза ПЖ (прототип) при внутримышечном введении 107250 ед или 0,33 мг / на 1 г массы не приводит к выживанию животных.
Используемая доза заявляемой РНКазы Bi (30000 ед/мл или 0,035 мг/мл) в 3,6 раз меньше дозы прототипа РНКазы ПЖ (107250 ед/мл или 0,33 мг/мл) по активности (107250 ед. 30000 ед = 3,6) и в 9,4 раза меньше по содержанию белка (0,33 мг. 0,035 мг = 9,4). Противовирусное действие РНКазы Bi в отношении ВБА имеет четкую зависимость доза-эффект, тогда как РНКаза ПЖ (прототип) в исследованных концентрациях, значительно превышающих концентрации РНКазы Bi по активности и по белку, не приводит к выживанию животных, но увеличивает продолжительность их жизни, что свидетельствует о слабой противовирусной активности РНКазы ПЖ.
Таким образом, данные по противовирусному действию РНКазы Bi in vivo свидетельствуют о том, что РНКаза Bi обладает способностью подавлять размножение ДНК-содержащих вирусов, например вируса болезни Ауески, что находится в соответствии с результатами in vitro (таблица 2).
Пример 6. Оценка противовирусной активности РНКазы Bi и РНКазы ПЖ (прототип) при заражении вирусом гриппа куриных эмбрионов («in ovo»)
Оценку противогриппозной активности РНКаз «in ovo» проводят на 10-дневных развивающихся куриных эмбрионах [5]. Препарат вводят по профилактической схеме, т.е. за 1 час до инокуляции вируса, и по лечебной схеме, т.е. через 1 час после инокуляции вируса. Инфицирующая доза вируса - 100 ЭИД/0,2 мл (ЭИД - эмбриональная инфекционная доза); ферменты вводят в дозе 150000 ед/эмбрион (Таблица 6).
Противовирусная активность сравниваемых рибонуклеаз (заявляемого и прототипа) оценивается в равных дозах по активности, но доза РНКазы ПЖ по белку равна 0,5 мг на эмбрион, а доза РНКазы Bi - 0,2 мг на эмбрион, т.е. доза РНКазы ПЖ по белку в 2,5 раза больше. Противовирусная активность РНКазы Bi и РНКазы ПЖ в отношении штаммов вируса гриппа A/PR/8/34, выраженная индексом защиты (ИЗ) независимо от схемы лечения для обоих ферментов, достоверно не различается и находится в диапазоне 67-71,2% выживших эмбрионов при заражающей дозе 100 ЭИД (Таблица 6).
Противовирусная эффективность РНКазы Bi и РНКазы ПЖ в отношении штаммов вируса гриппа А (Одесса) 2882/82 в равных дозах по активности и вводимых по профилактической схеме достоверно не различается - ИЗ равен 70,8-72%, ИЗ для лечебной схемы равен 76,0-77,7% (Таблица 6). С учетом различий в дозах вводимых ферментов по ферментому белку противовирусная эффективность РНКазы Bi в 2,5 раза выше эффективности РНКазы ПЖ (прототипа).
РНКаза Bi обладает эффективностью в отношении человеческого вируса гриппа типа В (Таблица 7).
Противовирусная активность заявляемой РНКазы Bi в отношении вируса гриппа В (В/Ленинград/369/75) при заражении вирусом гриппа куриных эмбрионов «in ovo». Инфицирующая доза вируса - 1080 ЭИД50 /0,2 мл (эмбриональных инфицирующих доз, вызывающих гибель 50% эмбрионов). - РНКаза Bi в дозе 0,5 мг/эмбрион
И3 - Индекс защиты рассчитывают по формуле: ИЗ=((Мс-Ме)/Мс)×100%, где
Мс и Ме - смертность в контрольной и опытной группе соответственно
Антивирусная активность, индекс защиты (И3)%
Противовирусная активность РНКазы Bi в отношении вируса гриппа В при инфицирующей дозе вируса 1080 ЭИД50 /0,2 мл независимо от способа лечения колеблется в диапазоне ИЗ 65-67%. Данные о влиянии РНКазы ПЖ на инфекцию, вызванную вирусом гриппа В, отсутствуют (не обнаружены).
Пример 7. Оценка противовирусной активности РНКазы Bi и РНКазы ПЖ (прототип) при заражении вирусом гриппа мышей
Оценку противогриппозной активности на белых беспородных мышах [5] весом 16-18 г проводят следующим образом. Используют лечебно-профилактическую схему введения препарата внутримышечно, т.е. за 24 и 1 час до инфицирования, а также через 24, 48 и 72 часа после интраназального инфицирования животных под легким эфирным наркозом [5]. Разовая доза РНКаз - 750000 ед/кг. Инфицирующая доза вируса 5 ЛД50 /0,05 мл (Таблица 8).
Противогриппозная активность заявляемой РНКазы Bi и РНКазы ПЖ (прототип) при инфицировании белых мышей вирусом гриппа A/PR /8/34. ИЗ - Индекс защиты рассчитывают по формуле: ИЗ=((Мс-Ме)/Мс)×100%, где Мс и Me - смертность в контрольной и опытной группе соответственно
Способ введения препаратов
Разовая доза препарата в мг/кг
Количество мышей в группе
При лечении по лечебно-профилактической схеме РНКазой Bi мышей, инфицированных 5 ЛД50 вируса A/PR/8/34, дозой фермента 750000 ед или 1,0 мг/кг в течение 5 суток, индекс защиты равен 67,7%. РНКаза ПЖ в дозе 750000 ед или 2,5 мг/кг, используемая для лечения по той же схеме, противогриппозной активностью не обладала.
Приведенные примеры 1, 2, 3, 4, 5, 6, 7 проявления противовирусной эффективности рибонуклеаз наглядно свидетельствуют о том, что РНКаза Bi, с учетом различия в используемых дозировках ферментов и эффективности подавления размножения вирусов, активнее прототипа - РНКазы ПЖ (панкреатического фермента).
Например, эффективность подавления размножения вируса ящура (ВЯ) РНКазой Bi (заявляемый) по сравнению с РНКазой ПЖ (прототип) с учетом различий в конечных титрах вируса и различиях в дозах заявляемого фермента и прототипа в 9 раз выше по активности и в 21 раз по белку (Пример 1, Таблица 1).
Эффективность подавления размножения ВБА РНКазой Bi (заявляемый фермент) по сравнению с РНКазой ПЖ (прототип) с учетом различий в конечных титрах вируса и различиях в дозах заявляемого фермента и прототипа выше в 12 раз по активности и в 28 раз по белку (Пример 2, Таблица 2).
Заявляемая РНКаза Bi с учетом различий в количестве выживших животных и различий в используемых дозах ферментов эффективнее РНКазы ПЖ (прототип) предотвращает гибель инфицированных вирусом ящура мышей в 15 раз по активности и 37,5 раз по ферментному белку (Пример 3, Таблица 3).
Заявляемая РНКаза Bi иного (по отношению к штамму Bacillus intermedius 7P) штамма с учетом различий в количестве выживших животных и различий в используемых дозах ферментов эффективнее противовирусной эффективности РНКазы ПЖ (прототип) предотвращает гибель инфицированных вирусом ящура кроликов по активности в 8 раз, по белку в 20 раз (Пример 4, Таблица 4).
Заявляемая РНКаза Bi эффективнее РНКазы ПЖ в отношении ДНК-содержащего вируса болезни Ауески (ВБА). РНКаза Bi в 3,6 раз меньшей дозе по сравнению с прототипом РНКазой ПЖ по активности и в 9,4 раза меньшей по содержанию белка обладает противовирусной эффективностью в отношении ВБА и имеет четкую зависимость доза-эффект. РНКаза ПЖ (прототип) в исследованных концентрациях, значительно превышающих концентрации РНКазы Bi по активности и по белку, не приводит к выживанию животных, увеличивая только продолжительность их жизни (Пример 5, Таблица 5). Это свидетельствует о слабой противовирусной активности РНКазы ПЖ в отношении ДНК-содержащего вируса.
Противогриппозная эффективность РНКазы Bi и РНКазы ПЖ «in ovo» (при заражении вирусом гриппа А куриных эмбрионов), оцениваемая в равных дозах по активности, достоверно не различается. Однако доза вводимого в эмбрионы ферментного белка РНКазы Bi в два с половиной раза меньше. Противогриппозная эффективность РНКазы Bi, оцениваемая количеством ферментного белка, вводимого в эмбрионы, в 2,5 раза выше противовирусной эффективности РНКазы ПЖ (Пример 6, Таблица 6).
РНКаза Bi подавляет размножение не только вируса типа А, но и вируса типа В. Данные о способности РНКазы ПЖ подавлять размножение вируса типа В отсутствуют (Пример 6, Таблица 7).
При лечении РНКазой Bi мышей, инфицированных вирусом гриппа А, индекс защиты животных составил 67,7% (при летальности 25%). Панкреатическая РНКаза ПЖ в этой же дозе по активности (в 2,5 раза большей по ферментному белку) по индексу защиты не активна (летальность 81,8%) (Пример 7, Таблица 8).
Аналогичные результаты подавления размножения вирусов получены при использовании РНКазы другого штамма Bacillus intermedius, структурно идентичной РНКазе исходного штамма Bacillus intermedius 7P, описанного в вышеупомянутых примерах (пример 4).
Приведенные примеры предполагаемого изобретения показывают его полезность для медицины и ветеринарии. Преимущества заявляемой РНКазы (РНКазы Bacillus intermedius) no сравнению с прототипом (панкреатической РНКазой ПЖ) заключаются в следующем.
1. Подавление размножения вирусов РНКазой Bacillus intermedius достигается при использовании более низких доз фермента (для млекопитающих in vivo в 12,0-20,0 раз ниже по ферментативной активности, и в 20,0-37,5 раз ниже по ферментному белку), вводимых в инфицированный организм. Это позволяет уменьшить количество фермента, которое необходимо ввести в организм для достижения необходимого эффекта подавления размножения вирусов. Уменьшение количества вводимого в организм фермента уменьшает риск иммунных осложнений, вызываемых вводимым в организм чужеродным белком; кроме того, соответственно уменьшается риск стимуляции ферментом аллергенных свойств других веществ, попадающих в организм на фоне введения РНКазы. Эти факторы повышают результативность и эффективность лечебного процесса.
2. Производство бактериальной РНКазы Bacillus intermedius может функционировать стабильно, вне зависимости от наличия, местонахождения, сезона и загруженности мясокомбинатов, поставщиков сырья для производства прототипа - панкреатической РНКазы.
3. Производство заявляемой РНКазы Bacillus intermedius может быть размещено вне зависимости от расположения мясокомбинатов - поставщиков сырья для прототипа.
4. Применение РНКазы Bacillus intermedius для подавления размножения вирусов позволяет исключить дефицит РНКазы как лекарственного препарата, обеспечивает потребности медицины и ветеринарии в РНКазе - средстве для лечения вирусных инфекций.
Предлагаемое изобретение удовлетворяет критериям новизны, так как заявляемый способ использования РНКазы Bacillus intermedius для подавления размножения вирусов реализуется при существенно меньших по сравнению с прототипом дозах применения и подавляет размножение вирусов существенно действеннее аналогов и прототипа.
Способ использования РНКазы Bacillus intermedius для подавления размножения вирусов имеет изобретательский уровень, поскольку не выявлены способы использования других РНКаз для подавления размножения вирусов с такой же эффективностью, как заявляемый способ использования РНКазы Bacillus intermedius. Заявляемый способ позволяет значительно результативнее (от 2 до 37 раз по сравнению с аналогами и прототипом) подавлять размножение вирусов в инфицированных организмах млекопитающих и других теплокровных животных.
Заявляемый способ позволяет применять ранее не известное средство для подавления размножения как РНК-, так и ДНК-содержащих вирусов у инфицированных млекопитающих и теплокровных животных. Выявление такого средства подавления размножения вирусов расширяет в медицине и ветеринарии перечень лекарственных средств (по сравнению с перечнем известных средств) для профилактики и борьбы с инфекционными заболеваниями вирусного происхождения.
Заявляемый способ - безопасный, применяемые при выделении бактериальной рибонуклеазы Bacillus intermedius компоненты абсолютно безвредны для человека. Способ позволяет успешно лечить млекопитающих и теплокровных животных от широкого перечня болезней вирусной природы - биологических объектов, недоступных для прототипа и аналогов, то есть заявленное изобретение обладает расширенной (по сравнению с прототипом) областью применения. Приведенные результаты применения заявляемого способа подтверждают его новизну. Заявляемый способ является осуществимым с применением стандартных технических устройств и оборудования в промышленном производстве лечебных препаратов, в деятельности организаций здравоохранения, животноводства. Это соответствует предъявляемому к изобретениям критерию «промышленная применимость».
Предлагаемый способ полезен и необходим для применения специалистам из области медицины и ветеринарии, например для профилактики и лечения вирусных заболеваний людей и животных. Примеры применения предлагаемого изобретения показывают его полезность. Применение предлагаемого способа расширяет перечень средств, используемых в лечебных целях, например при борьбе с острыми вирусными инфекциями.
Предлагаемое изобретение удовлетворяет критериям новизны, так как при определении уровня техники не обнаружено средство, которому присущи признаки, идентичные (то есть совпадающие по исполняемой ими функции и форме выполнения этих признаков) всем признакам, перечисленным в формуле изобретения, включая характеристику назначения.
Заявляемый способ использования рибонуклеазы Bacillus intermedius имеет изобретательский уровень, поскольку не выявлены технические решения, имеющие признаки, совпадающие с отличительными признаками данного изобретения, и не установлена известность влияния отличительных признаков на указанный технический результат.
Заявленное техническое решение можно реализовать в промышленном производстве лекарственных препаратов, в деятельности организаций фармацевтической промышленности, здравоохранения, животноводства посредством использования известных стандартных технических устройств и оборудования. Это соответствует критерию «промышленная применимость», предъявляемому к изобретениям.
2. Леонова Н.С. Применение бактериальной эндонуклеазы для оздоровления картофеля от вирусов. Леонова Н.С. Салганик Р.И. // Сибирский вестник сельскохозяйственной науки, 1991, № 5. - С.25-28.
3. Баталина Т.А. Лихошвай Е.В. Пензикова Г.А. Исследование влияния рибонуклеазы Actynomyces rimosus на репродукцию некоторых вирусов // Антибиотики, 1977, т.22, № 1, 25-28.
4. Лещинская И.Б. Нуклеодеполимеразы сапрофитных бактерий. - Казань: Изд-во Казанского университета, 1975, 180 с.
5. Штарке Г. Практическая вирусология. - М. Колос, 1970. - С, 126-128.
6. Карышва А.Ф. Сюрин В.Н. Руководство по практической вирусологии (Справочное пособие). - Кишинев: Изд-во «Штиница», 1980. - 212 с.
ФОРМУЛА ИЗОБРЕТЕНИЯ1. Способ использования рибонуклеазы бактериальной для подавления размножения вирусов, заключающийся в том, что для увеличения эффективности подавления размножения РНК- и ДНК-содержащих вирусов в инфицированном организме, для лечения острых вирусных заболеваний млекопитающих и теплокровных животных используют бактериальный фермент РНКазу Bacillus intermedius 7P.
2. Способ по п.1, отличающийся тем, что используют структурно идентичную РНКазе исходного штамма Bacillus intermedius 7P рибонуклеазу иных штаммов Bacillus intermedius - селекционированных, клонированных и инженерных штаммов.